L’aventure des premiers bébés génétiquement modifiés finit aussi mal qu’elle a commencé.
Après avoir été dénoncé par presque toute la communauté scientifique, le biologiste He Jiankui vient d’être condamné par la justice chinoise. L’histoire aura au moins eu une utilité : montrer tout ce qu’il ne faut pas faire en recherche et provoquer un débat de société sur les modifications génétiques chez les humains.
À la fin de 2018, He Jiankui a choqué la communauté scientifique en annonçant qu’il avait mis au monde des jumelles génétiquement modifiées. Cette percée a été annoncée aux médias sans être validée par des pairs et sans être publiée dans un journal scientifique reconnu. Et, selon la version officielle de Pékin, sans l’aval de son université ou du gouvernement.

PHOTO MARK SCHIEFELBEIN, ARCHIVES ASSOCIATED PRESS
Le biologiste chinois He Jiankui
Le 30 décembre dernier, le chercheur a reçu sa peine : trois ans de prison et une amende d’environ 500 000 $ pour « pratique illégale de la médecine ». Ses deux collaborateurs ont aussi été punis.
L’expérience posait en effet une multitude de problèmes éthiques et médicaux.
Le biologiste a utilisé la méthode CRISPR-Cas9 pour modifier le gène CCR5 de jumelles chinoises dont le père était porteur du VIH. Cela devait leur permettre de ne pas en être porteuses à leur tour.
Or, les avantages étaient incertains – les bébés n’allaient pas forcément être porteurs du VIH. Et les désavantages étaient potentiellement nombreux. La modification du CCR5 peut avoir certains effets indésirables, comme une vulnérabilité face au virus du Nil. Il arrive aussi que la technique CRISPR-Cas9 altère accidentellement d’autres gènes, créant des maladies aussi graves qu’un cancer.
En plus de risquer de nuire à la santé des bébés, les chercheurs chinois ont aussi violé les normes élémentaires d’éthique.
Selon une enquête du MIT Technology Review, l’équipe aurait falsifié les formulaires de consentement et menacé de faire payer les parents s’ils mettaient fin à l’expérience. La publication allègue aussi que l’expérience n’avait pas que des visées thérapeutiques. Elle pourrait aussi avoir amélioré des prédispositions des bébés – l’altération du CCR5 a déjà amélioré la mémoire chez des souris.
Bien sûr, il n’est pas le premier à avoir utilisé CRISP-Cas9 sur des humains. Mais les expériences précédentes portaient sur les cellules somatiques (non transmises aux descendants) de patients ou sur des cellules germinales (transmissibles aux descendants) d’embryons qui n’étaient pas destinés à naître. L’équipe chinoise était donc la première à proposer de modifier le patrimoine génétique de personnes réelles et de leurs descendants.
Ce fut un choc. En réaction, l’Organisation mondiale de la santé (OMS) a créé un comité pour encadrer cette science. Ses recommandations ont été publiées le printemps dernier. Parmi elles, on trouve la création d’un registre des recherches avec CRISP-Cas9 afin d’éviter que des chercheurs travaillent en cachette. Et aussi l’interdiction des modifications sur les cellules germinales pour des cas cliniques.
En effet, ces modifications comportent des risques énormes pour les patients.
Deux questions demeurent toutefois.
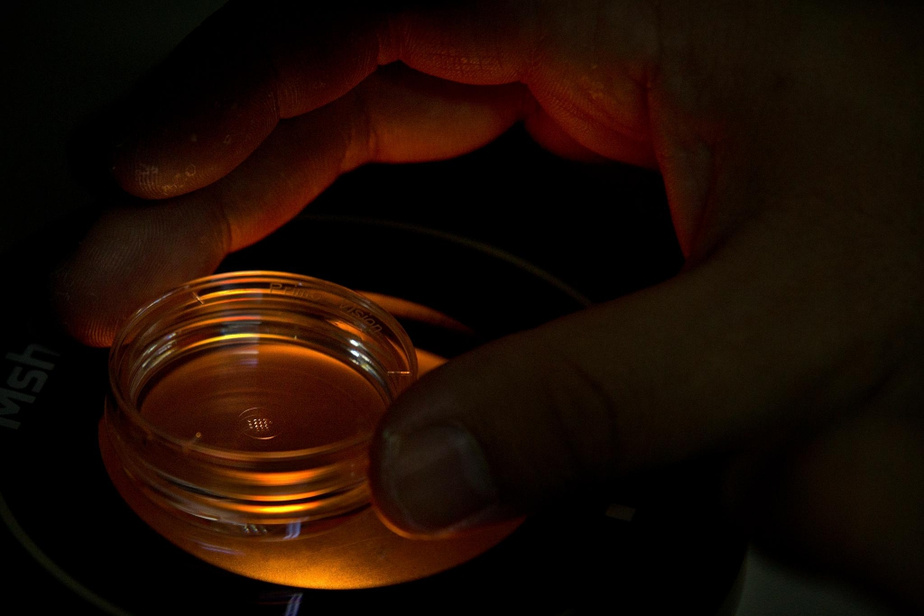
PHOTO MARK SCHIEFELBEIN, ARCHIVES ASSOCIATED PRESS
« L’expérience posait une multitude de problèmes éthiques et médicaux », souligne notre éditorialiste.
La première, c’est de savoir si les recherches précliniques sur des embryons non inséminés devraient être autorisées dès maintenant. Contrairement à plusieurs autres pays, le Canada répond non. Cela fait de notre pays un des plus conservateurs. Plusieurs scientifiques le déplorent et craignent que nous prenions du retard en recherche. Il est difficile de leur donner tort.
La seconde question porte sur l’avenir. Avec le temps, CRISP-Cas9 devrait devenir sécuritaire. Il faudra alors se demander si en l’absence de risque indu pour le patient, la technologie mérite d’être autorisée, et si oui, à quelles conditions. C’est à cela que réfléchit maintenant le groupe d’experts de l’OMS pour son prochain rapport.
L’année dernière, la Commission de l’éthique en science et en technologie du Québec a formulé ses recommandations. Si la technologie devient sécuritaire, son application devrait être limitée aux maladies graves pour lesquelles il n’existe pas d’autre traitement efficace. La Commission s’oppose aux modifications pour améliorer le génome, qui risquent d’aggraver les inégalités en ouvrant la voie à une humanité à deux vitesses.
En résumé, le débat s’articule autour de trois choix : les modifications sur les cellules somatiques ou les germinales, les recherches précliniques ou cliniques, et enfin les modifications pour guérir ou améliorer le génome. Sur papier, ces distinctions paraissent claires. Par contre, en laboratoire, les lignes risquent de s’embrouiller. Le débat est sensible et complexe, mais ce n’est pas une raison pour l’esquiver.
Espérons que le Canada et les autres pays industrialisés n’aient pas des lois trop différentes les uns des autres.
Et que la communauté scientifique se discipline pour condamner fermement les chercheurs en mal d’attention qui menacent la sécurité de leurs patients pour faire des coups de publicité, comme ce fut le cas avec He Jiankui. Les enjeux sont trop importants pour s’en remettre à l’anarchie scientifique.
Qu'en pensez-vous? Exprimez votre opinion

